جزيء هو جزيء مع كتلة الجزيئية العالية. تكوين جزيء
جزيء هو جزيء لديهارتفاع الوزن الجزيئي. ويمثل هيكلها في شكل تكرار المتكررة الروابط. دعونا ننظر في ملامح هذه المركبات، وأهميتها بالنسبة للنشاط الحيوي للكائنات الحية.

ملامح التكوين
وتتكون الجزيئات البيولوجية من مئات الآلاف من المواد الأولية الصغيرة. للكائنات الحية، وهناك ثلاثة أنواع رئيسية من الجزيئات: البروتينات، السكريات، والأحماض النووية.
مونومرات البداية بالنسبة لهمالسكريات الأحادية، النيوكليوتيدات، الأحماض الأمينية. جزيء ما يقرب من 90 في المئة من كتلة الخلية. اعتمادا على تسلسل بقايا الأحماض الأمينية، يتم تشكيل جزيء بروتين معين.
المواد عالية الجزيئية هي تلك التي لديها كتلة المولية أكبر من 103 دا.

تاريخ المظهر
متى يظهر جزيء؟ هذا المفهوم قدمه الحائز على جائزة نوبل في مجال الكيمياء من قبل هيرمان ستودينجر في عام 1922.
ويمكن النظر في ملف البوليمر في النموذجخيط متشابك تم تشكيله عن طريق الخطأ لفك الملف حول الغرفة. هذا تشابك بشكل منهجي يغير التشكل، وهذا هو التكوين المكاني للجزيء. وهو مشابه لمسار حركة براونية.
هناك تشكيل مثل هذا تشابك،أنه على مسافة معينة سلسلة البوليمر "يفقد" معلومات حول الاتجاه. الحديث عن التشابك يمكن أن يكون في حالة عندما تكون المركبات عالية الجزيئية على طول سيكون أكبر بكثير من طول الجزء الهيكلي.
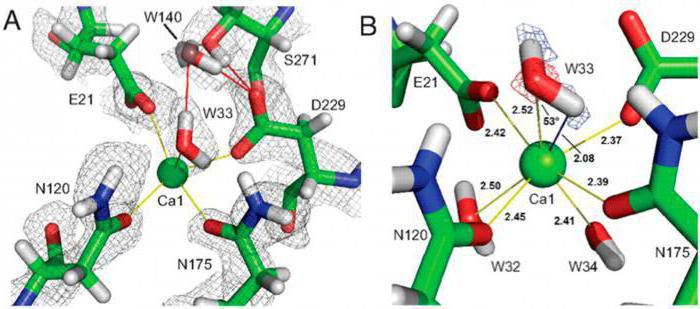
التكوين غلوبولار
جزيء هو التشكل كثيفة، فيفمن الممكن لمقارنة حجم جزء من البوليمر مع وحدة. تتحقق الحالة الكروية في تلك الحالات عندما ينشأ الجاذبية المتبادلة بين الروابط الفردية للبوليمرات مع بعضها البعض والبيئة الخارجية.
نسخة طبق الأصل من هيكل جزيء هو أن جزءا من المياه التي بنيت في كعنصر من هذا الهيكل. هو أقرب البيئة المائية من جزيء.
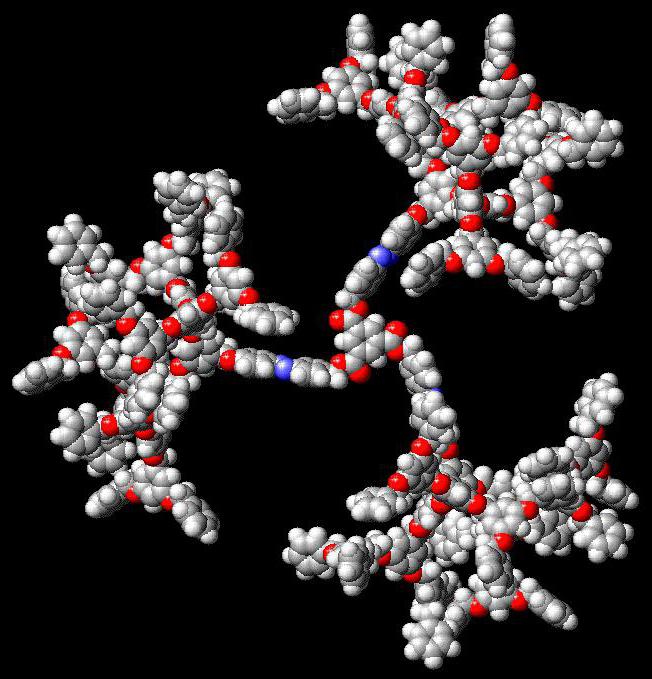
خصائص جزيء البروتين
جزيئات البروتين هي ماءالمواد. عندما يذوب في الماء، والبروتين الجاف، في البداية تتضخم، ثم هناك انتقال تدريجي إلى الحل. خلال تورم، جزيئات الماء تدخل داخل البروتين، ملزمة هيكلها إلى مجموعات القطبية. في هذه الحالة، يتم تخفيف التعبئة وثيقة من سلسلة ببتيد. ويعتبر جزيء البروتين المنتفخ هو الحل العكسي. مع امتصاص لاحق من جزيئات الماء، يتم فصل جزيئات البروتين من الكتلة الإجمالية، وعملية حل أيضا يأخذ مكان.
ولكن تورم جزيء البروتين لا يؤدي في جميع الحالات إلى حل. على سبيل المثال، الكولاجين بعد امتصاص جزيئات الماء لا يزال في حالة تورم.
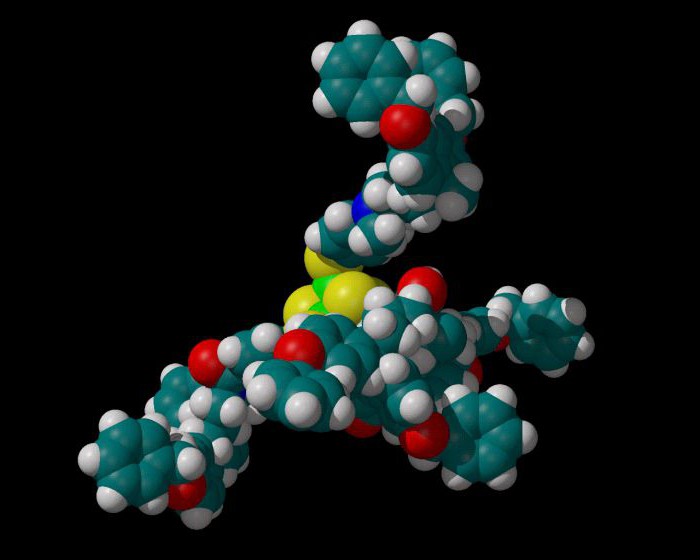
هيدرات النظرية
المركبات عالية الجزيئية وفقا لهذه النظرية ليست كذلكتمزج ببساطة، يحدث الربط الكهربائي من جزيئات الماء مع شظايا القطبية من الجذور الجانبية من الأحماض الأمينية التي لديها شحنة سالبة، وكذلك الأحماض الأمينية الأساسية التي تحمل شحنة موجبة.
ويرتبط الماء المائي جزئيا بمجموعات الببتيد التي تشكل روابط هيدروجينية مع جزيئات الماء.
على سبيل المثال، الببتيدات التي تحتوي علىالمجموعات الجانبية غير القطبية. عندما تكون ملزمة لمجموعات الببتيد، فإنه يقسم سلاسل ببتيد. وجود الجسور بين الشظايا لا يسمح للجزيئات البروتين أن يكسر تماما، لتمرير في شكل حل.
هيكل الجزيئات ينهار عند تسخينها، مما أدى إلى تمزق والافراج عن سلاسل ببتيد.
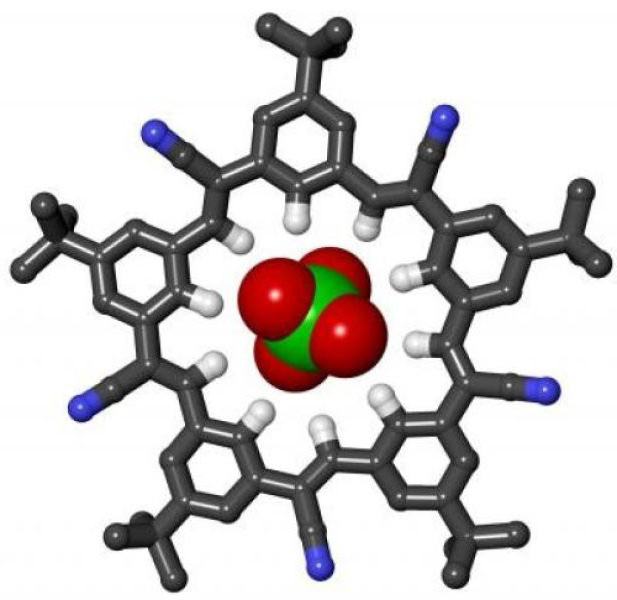
الجيلاتين الميزات
وفقا للتركيب الجيلاتين الكيميائي يشبه الكولاجين، فإنه يشكل السائل لزج بالماء. ومن بين الخصائص المميزة للجيلاتين، يمكن تمييز قدرته على تشكيل هلام.
وتستخدم هذه الأنواع من الجزيئات كعامل مرقئ وعوامل بديلة للبلازما. يتم استخدام قدرة الجيلاتين لتشكيل المواد الهلامية في تصنيع كبسولات في صناعة المستحضرات الصيدلانية.
التفرد للذوبان الجزيئات
هذه الأنواع من الجزيئات مختلفةالذوبان في الماء. يتم تحديده من قبل تكوين الأحماض الأمينية. في وجود الأحماض الأمينية القطبية في الهيكل، والقدرة على حل في الماء هو زيادة كبيرة.
كما تتأثر هذه الميزة بالميزةمنظمة جزيء. في البروتينات الكروية، والذوبان أعلى من الجزيئات ليفية. في تجارب عديدة كان الاعتماد على الخصائص حل المذيبات المستخدمة.
الهيكل الأساسي لكل جزيء البروتين هو مختلف، مما يعطي البروتين الفردية للخصائص. وجود كروسلينكس بين سلاسل ببتيد يقلل من الذوبان.
ويتكون الهيكل الأساسي للجزيئات البروتين بسبب الببتيد (أميد) السندات، مع تدميرها، يحدث تمسخ البروتين.
التمليح
لزيادة ذوبان جزيئات البروتينيتم استخدام حلول الأملاح المحايدة. على سبيل المثال، وبهذه الطريقة، يمكن إجراء هطول انتقائي للبروتينات، ويمكن تنفيذ تجزئتها. كمية الجزيئات التي تم الحصول عليها تعتمد على التكوين الأولي للخليط.
خصوصية البروتينات، التي يتم الحصول عليها عن طريق التمليح، ويتكون في الحفاظ على الخصائص البيولوجية بعد إزالة كاملة من الملح.
جوهر العملية هو إزالة الأنيونات والكاتيونات من الملح من البروتين قذيفة رطبة، مما يضمن استقرار جزيء. ويملح الحد الأقصى لعدد جزيئات البروتين باستخدام الكبريتات. ويستخدم هذا الأسلوب لتنقية وفصل الجزيئات البروتين، لأنها تختلف بشكل كبير في حجم المسؤول، هيدرات المعلمات قذيفة. كل بروتين لديه منطقة التمليح الخاصة بها، وهذا هو، فإنه يحتاج إلى تحديد ملح تركيز معين.
الأحماض الأمينية
في الوقت الحاضر، ما يقرب من مائتي الأحماض الأمينية معروفة التي هي جزء من جزيئات البروتين. اعتمادا على هيكل، وتنقسم إلى مجموعتين:
- بروتين، التي هي جزء من الجزيئات.
- غير بروتينية، لا تأخذ دورا نشطا في تشكيل البروتينات.
نجح العلماء في فك رموز التسلسلوالأحماض الأمينية في العديد من جزيئات البروتين من أصل الحيوان والنبات. بين الأحماض الأمينية، والتي غالبا ما توجد في جزيئات البروتين، نلاحظ سيرين، الجلايسين، ليوسين، ألانين. ويتميز كل بوليمر بيولوجي طبيعي من خلال تكوين الأحماض الأمينية الخاصة به. على سبيل المثال، تشمل بروتامينس حوالي 85 في المئة أرجينين، ولكن ليس لديهم الأحماض الأمينية الحمضية، دوري. فيبروين هو جزيء البروتين من الحرير الطبيعي، الذي يحتوي على حوالي نصف الجليكاين. في الكولاجين هناك مثل الأحماض الأمينية النادرة كما هدروكسيبرولين، هيدروكسيليزين، غائبة في جزيئات البروتين الأخرى.
يتم تحديد تكوين الأحماض الأمينية ليس فقط من خلال خصائص الأحماض الأمينية، ولكن أيضا من خلال وظائف، عن طريق تعيين جزيئات البروتين. يتم تحديد تسلسلها بواسطة الشفرة الوراثية.
مستويات التنظيم الهيكلي للبوليمرات الحيوية
هناك أربعة مستويات: الابتدائي والثانوي، العالي، ورباعي. كل هيكل له خصائصه المميزة.
الهيكل الأساسي لجزيئات البروتين هو سلسلة ببتيد خطي من بقايا الأحماض الأمينية المرتبطة بسندات الببتيد.
هو هذا الهيكل الذي هو الأكثر استقرارا، لأنه يحتوي على الروابط التساهمية الببتيد بين مجموعة الكربوكسيل من واحد من الأحماض الأمينية ومجموعة الأمينية من جزيء آخر.
الهيكل الثانوي ينطوي على وضع سلسلة ببتيد مع مساعدة من الروابط الهيدروجين في شكل حلزوني.
يتم الحصول على النوع الثالث من البوليمر الحيوي عن طريق التعبئة المكانية للببتيد. أشكال لولبية ومطوية مغلفة من الهياكل الثلاثية تقسيم فرعي.
للبروتينات كروية الشكل بيضاوي الشكل المميز، وييفي الجزيئات التي تتميز شكل ممدود.
إذا كان جزيء يحتوي على واحد فقطسلسلة ببتيد، والبروتين له هيكل ثالث فقط. على سبيل المثال، هو بروتين من الأنسجة العضلية (ميوغلوبين)، اللازمة لربط الأوكسجين. يتم بناء بعض البوليمرات الحيوية من عدة سلاسل ببتيد، ولكل منها هيكل ثالثي. في هذه الحالة، جزيء له بنية الرباعية تتكون من عدة الكريات، متحدة في هيكل كبير. الهيموجلوبين يمكن اعتبار البروتين الرباعي الوحيد الذي يحتوي على حوالي 8 في المئة من الهستيدين. فمن العازلة داخل الخلايا النشط في كرات الدم الحمراء، والذي يسمح الحفاظ على قيمة الرقم الهيدروجيني للدم على مستوى مستقر.
الأحماض النووية
وهي مركبات جزيئية عالية،والتي تتشكل من شظايا من النيوكليوتيدات. تم العثور على الحمض النووي الريبي والحمض النووي في جميع الخلايا الحية، فإنها تؤدي وظيفة التخزين، ونقل، فضلا عن تنفيذ المعلومات الوراثية. المونومرات هي النيوكليوتيدات. كل واحد منهم لديه في تكوين ما تبقى من القاعدة النيتروجينية والكربوهيدرات، وكذلك حمض الفوسفوريك. وقد أظهرت الدراسات أن مبدأ التكامل لوحظ في الحمض النووي للكائنات الحية المختلفة. الأحماض النووية قابلة للذوبان في الماء، ولكن لا تذوب في المذيبات العضوية. وتدمر هذه البوليمرات الحيوية عندما ترتفع درجة الحرارة، والأشعة فوق البنفسجية.
بدلا من الختام
بالإضافة إلى البروتينات المختلفة والأحماض النووية،الجزيئات هي الكربوهيدرات. السكريات في تكوينها لديها المئات من المونومرات، التي لها طعم حلو لطيف. وكمثال على الهيكل الهرمي للجزيئات الكبيرة، يمكن للمرء أن يذكر جزيئات ضخمة من البروتينات والأحماض النووية مع الوحدات الفرعية المعقدة.
على سبيل المثال، الهيكل المكاني من كرويجزيء البروتين هو نتيجة للتنظيم الهرمي متعدد المستويات للأحماض الأمينية. بين المستويات الفردية هناك علاقة وثيقة، ترتبط عناصر من مستوى أعلى مع الطبقات السفلى.
جميع البوليمرات الحيوية تؤدي وظيفة مماثلة هامة. وهي اللبنات الأساسية للخلايا الحية ، وهي مسؤولة عن تخزين ونقل المعلومات الوراثية. بالنسبة لكل مخلوق حي ، فإن بروتينات معينة هي خاصية مميزة ، وبالتالي فإن علماء الكيمياء الحيوية يواجهون مهمة معقدة ومسؤولة ، يحلونها ، ويقومون بحفظ الكائنات الحية من موت معين.
</ p>



